 肾脏类器官培养案例 | 人肾脏类器官培养手册
肾脏类器官培养案例 | 人肾脏类器官培养手册
14331
2023-03-23
肾脏是人体中重要器官之一,具有清除代谢废物,维持电解质平衡等生理功能,保证机体内环境的稳定。肾脏类器官(kidney organoid)是肾脏功能的3D模型,有利于人类肾脏疾病的建模,大多由多能人类干细胞(PSC)在体外经诱导生成,能够表达出和人肾单位相似的各类结构,如肾小球足细胞、近端小管、远端小管、集合管等。
我们根据Nat Protoc.[1]发表的文章,整理了人类多能干细胞生成肾脏类器官的培养方案。
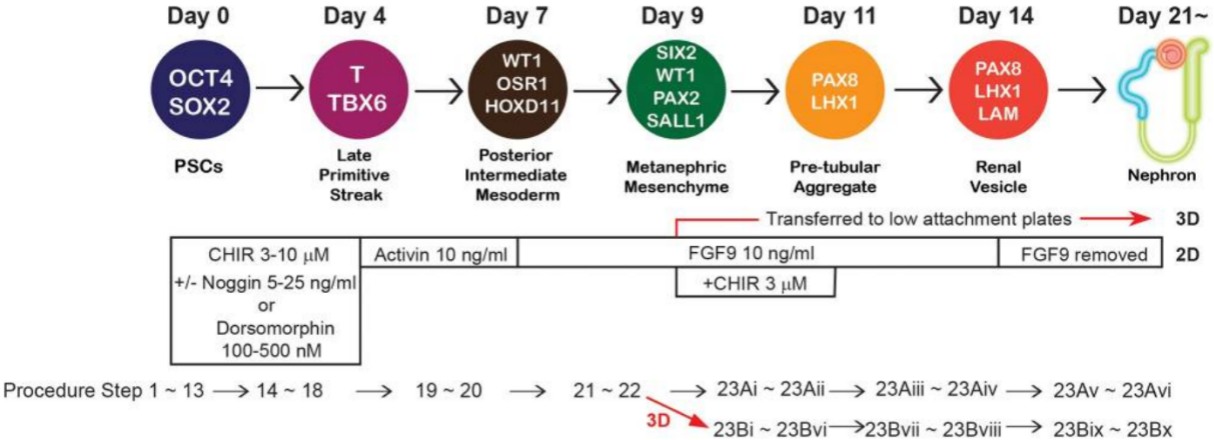
图1.hPSC分化为肾脏类器官的过程(PMID: 28005067)[1]
hPSC接种到包被了无LDEV低生长因子基底膜基质的6孔板上,用ReproFF2培养基(含有10 ng/mL FGF2)培养。健康的未分化hPSC显示出边界清晰的圆形集落形态,使用iPS细胞的解离溶液分离健康的未分化hPSC,每七天传代。
当细胞密度达到80%时,使用Accutase消化细胞,用ReproFF2培养基(含10 μM Y-27632(Cat# 53006ES)或Y-27632 dihydrochloride(Cat# 52604ES))重悬,接种到包被了无LDEV低生长因子基底膜基质的24孔板上,培养3天,更换为Advanced RPMI 1640培养基(含有1× L-GlutaMAX,3~10 μM CHIR-99021,5-25 ng/mL Noggin,100-500 nM Dorsomorphin)继续培养,每两天换液,直至细胞形态为松散形成的密集细胞团(一般需要96 h)。然后更换为Advanced RPMI 1640培养基(含有1× L-GlutaMAX,10 ng/mL activin A)继续培养2-3天。
更换为Advanced RPMI 1640培养基(含有1× L-GlutaMAX,10 ng/mL FGF9)继续培养2天。
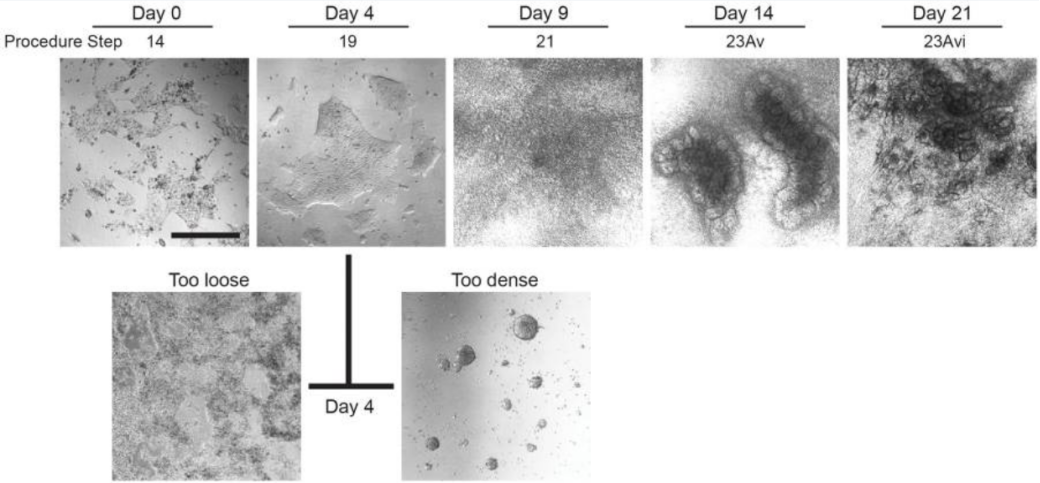
图2.hPSC分化过程中的形态变化(PMID: 28005067)[1]
Day 0,分化开始时未分化的hPSC (H9);Day 4,晚期原始条纹阶段;Day 9,肾单位祖细胞期. Day 14,肾囊泡期;Day 21,肾单位期;在第4天进行激活素A处理的细胞的最佳形态是可见松散密集的簇。
4.1 NPC向肾脏类器官的分化(2D)
步骤3后更换为Advanced RPMI 1640培养基(含有1× L-GlutaMAX,10 ng/mL FGF9,3 μM CHIR-99021)继续培养2天;然后更换为Advanced RPMI 1640培养基(含有1× L-GlutaMAX,10 ng/mL FGF9)培养2-3天,如果观察到类似肾小泡的带有管腔的圆极化结构,则继续下一步。如果在3天内未观察到肾泡结构,则通过免疫染色确认LHX1是否表达;然后更换为Advanced RPMI 1640培养基(含有1× L-GlutaMAX)培养,每2-3天换液,肾脏类器官在至少长达3个月的分化中是稳定的,肾单位结构可以用显微镜识别。
4.2 hPSC向肾脏类器官的分化(3D)
步骤2后使用Accutase消化细胞,用Advanced RPMI 1640培养基(含有1× L-GlutaMAX,10 ng/mL FGF9,3 μM CHIR-99021)重悬后接种于超低吸附的圆底96孔板中,培养2天,然后更换为Advanced RPMI 1640培养基(含有1× L-GlutaMAX,10 ng/mL FGF9)继续培养2-3天,直到显微镜观察到肾泡状圆形结构。
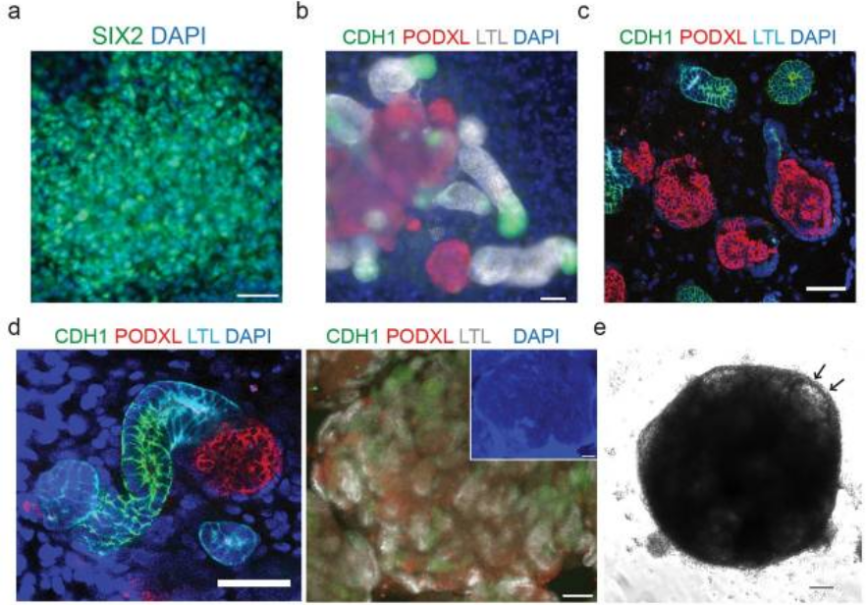
图3.NPC和肾单位的免疫染色(PMID: 28005067)[1]
(a)分化第9天SIX2的免疫荧光显示NPC。比例尺:50 μm;(b)免疫荧光染色鉴别分化2D培养中第21天的肾单位结构。比例尺:50 μm;(c) 在3D培养中分化的第21天用冷冻切片识别肾单位结构,比例尺:50 μm;(d) 3D培养中第28天(左,比例尺:50 μm)和第21天(右,比例尺100 μm)肾单位的免疫染色,PODXL:一种足细胞标记物,LTL:一种近端小管标记物,CDH1:Henle环和远端小管标记物;(e)3D培养中第21天类器官的明场图像,箭头表示肾小球结构。
Melissa H. Little团队于Nature Protocols发表研究,提出一种优化方案:通过延长分化周期并使用CDBLY2培养基,增强后肾祖细胞定向分化及肾单位祖细胞自我更新能力,从而从人多能干细胞高效构建近端肾小管功能强化的肾类器官[3]。
1. 细胞铺板与初始诱导(第0-5天)
将人多能干细胞(hPSCs)以每孔25,000个的密度接种于Laminin-521包被的培养板。第0天,在确认细胞状态良好、未出现自发分化且密度合适后,移除E8培养基,加入含6 µM CHIR-99021的E6培养基(1 mL/孔)。将细胞置于CO₂培养箱中培养,每48小时更换新鲜E6/CHIR培养基,持续至第5天。
2. FGF9诱导期(第5-8天)
第5天起,将培养基更换为添加200 ng/mL FGF9和1 µg/mL肝素的E6培养基,每2-3天换液。此阶段旨在促进后肾谱系定向分化。
3. CDBLY2扩增期(第8-13天)
从第8天开始,改用CDBLY2培养基进行每日换液,直至第13天。期间需持续镜检监测,确保细胞未发生上皮化,以保证后续三维培养的成功率。
4. 3D成熟类器官培养期(第13-27天)
吸除CDBLY2培养基,先用1 mL TrypLE Select清洗细胞,再加入新鲜TrypLE Select孵育3分钟。收集细胞后离心,将细胞微团(每孔3个)转移至Transwell膜表面。向Transwell下室加入含5 µM CHIR-99021的E6培养基,37°C孵育1小时完成CHIR脉冲处理。随后更换为含200 ng/mL FGF9和1 µg/mL肝素的E6培养基,继续培养至第18天。第18天后,改用不含FGF9和肝素的E6培养基,隔天换液,直至第27天获得成熟肾类器官。
图4 近端肾小管增强肾类器官构建流程
|
产品名称 |
产品编号 |
规格 |
简介 |
|
53006ES |
1 mg/5 mg/10 mg |
ROCK抑制剂 |
|
|
53003ES |
2 mg/5 mg/10 mg |
GSK-3α/β抑制剂 |
|
|
53593ES |
5 mg/25 mg |
AMPK选择性抑制剂 |
|
|
92528ES |
5 μg/100 μg/500 μg |
重组蛋白 |
|
|
91702ES |
10 μg/100 μg/500 μg |
重组蛋白 |
|
|
91305ES |
5 μg/100 μg/500 μg |
重组蛋白 |
|
|
91306ES |
5 μg/100 μg/500 μg |
重组蛋白 |
|
|
91330ES |
10 μg/100 μg/500 μg |
重组蛋白 |
|
|
40506ES |
100 mL |
细胞消化液 |
|
|
738416ES |
100 mg |
细胞培养添加剂 |
|
|
60701ES |
100 mL |
细胞培养添加剂 |
永利3044集团官网提供完善的小分子化合物系列产品,永利3044集团官网小分子化合物优势:
 产品经严格质检,品质有保障
产品经严格质检,品质有保障 产品纯度高,生化数据全
产品纯度高,生化数据全 产品有完善的售后
产品有完善的售后  产品种类全,可定制,一次买齐实验所需
产品种类全,可定制,一次买齐实验所需 可申请“发文章赢奖励”活动
可申请“发文章赢奖励”活动
选购yeasen小分子,发表文献拿奖励,paper任你发,奖励任你拿!
另针对类器官、干细胞等应用场景,永利3044集团官网均可提供完整解决方案:
[1] Morizane R, et al. Generation of nephron progenitor cells and kidney organoids from human pluripotent stem cells. Nat Protoc. 2017 Jan;12(1):195-207.
[2] Little MH, et al. Generating Kidney from Stem Cells. Annu Rev Physiol. 2019 Feb 10;81:335-357.
(本文中的实验方案基于已发表文献优化整理,内容仅供参考,实际实验条件可能因细胞系差异、实验室环境等因素需调整,建议用户在正式实验前进行预实验优化。)





